破解細胞膜磷脂調控助攻癌細胞移動 台大研究登國際期刊
2026/03/28 12:58 記者林曉雲/台北報導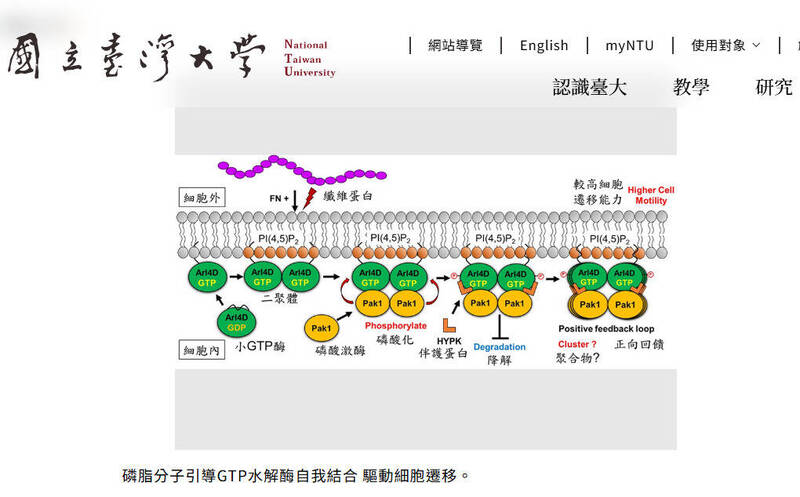
台大醫學院分子醫學研究所教授李芳仁研究團隊近日在國際期刊「美國國家科學院院刊」發表最新研究。(記者林曉雲翻攝台大官網)
細胞如何接收外部刺激、啟動移動,是生物醫學界的重要課題,因為細胞遷移不僅攸關胚胎發育、傷口修復,也與癌細胞侵襲轉移密切相關。國立台灣大學醫學院分子醫學研究所教授李芳仁研究團隊近日在國際期刊「美國國家科學院院刊」發表最新研究,首度揭示細胞外基質成分「纖連蛋白」可透過改變細胞膜上的磷脂環境,促使小型GTP水解酶Arl4D在膜上自我結合,進一步放大訊號並驅動細胞遷移,為理解癌症轉移機制提供新的分子線索。
研究團隊指出,過去學界已知Ras等小型GTP水解酶的聚集,是細胞訊號傳遞的重要機制,但單一蛋白如何在複雜細胞膜環境中穩定聚集、再把外界刺激轉為細胞運動指令,仍有許多關鍵環節未明。李芳仁團隊長期研究Arl4家族蛋白在癌細胞遷移中的角色,這次進一步鎖定Arl4D,解析它如何在纖連蛋白刺激下被啟動。
研究發現,當癌細胞感受到並附著於纖連蛋白時,細胞膜局部的PI(4,5)P2磷脂濃度會升高,吸引更多Arl4D聚集到膜上,形成初步自我結合;接著,蛋白激酶Pak1再對Arl4D進行磷酸化,兩股力量協同作用,使Arl4D形成更穩定的自我結合,並與Pak1組成穩定複合體,啟動後續引導細胞遷移的胞內訊號。研究團隊形容,這種機制像是替細胞內部的移動訊號裝上「擴音器」,讓遷移訊號被放大並延長。
李芳仁表示,這項發現解開過去對小型GTP水解酶如何穩定、放大訊號的疑問,也證實細胞外基質不只是提供支撐,還能透過調控磷脂與蛋白質結構互動,精準決定細胞命運,不僅有助理解正常生理中的細胞移動,也為癌細胞侵襲與轉移研究開啟新的可能治療方向。
這項研究主要由博士班學生張庭瑋執行,並獲國科會與國衛院長期經費支持。由於癌症轉移是臨床治療最棘手的問題之一,此次成果也被視為從基礎分子機制切入、尋找未來抗轉移新標的的重要進展。


















