國外疫苗沒做第三級試驗取得授權? 王婉諭盼政府精確說明
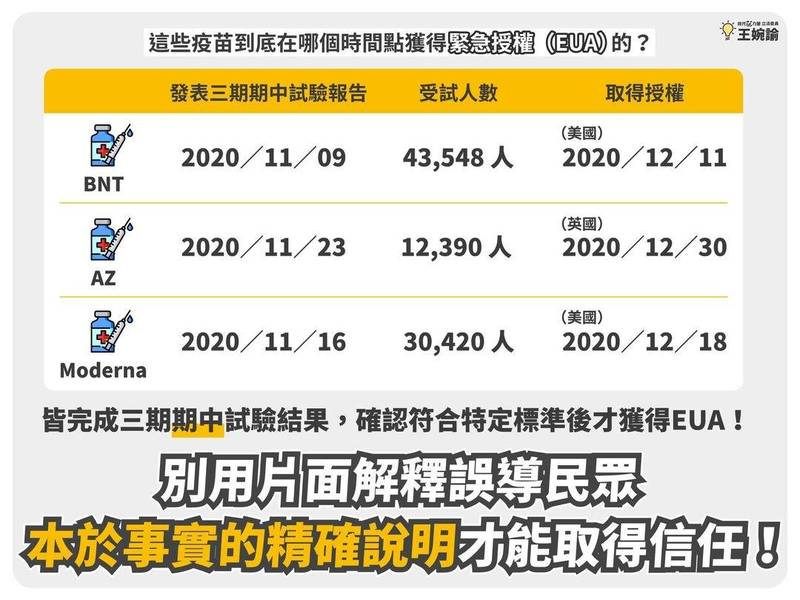
時代力量立委王婉諭今表示,AZ、BNT、莫德納3種疫苗都是完成三期期中試驗結果後,才獲得緊急授權。(翻攝自王婉諭臉書)
〔記者吳書緯/台北報導〕武漢肺炎本土疫情嚴峻,各界企盼國產疫苗早日投入施打,也引發何時可獲得緊急授權的爭論;時代力量立委王婉諭今表示,AZ、BNT、莫德納3種疫苗都是完成三期期中試驗結果後,才獲得緊急授權(EUA),批評指揮中心用片面資訊誤導民眾,應精確說明事實,並提醒執政黨不應將尚未完成二期解盲的國產疫苗,就計入台灣8月可取得的疫苗當中。
王婉諭今天透過臉書發文指出,近期對於海外疫苗的認證掀起論戰,許多人提到「AZ、BNT、Moderna都是做了三期試驗,才得到主要國家緊急授權的」,而指揮中心昨在記者會表示「AZ、BNT、Moderna等各家疫苗都是在完成第三期試驗前,即取得主要國家緊急授權的」。
針對兩者說法誰對誰錯,王婉諭表示,「這兩邊都只挑了想要呈現的事實來解釋,不僅不完整,也不夠精確」;王婉諭指出,AZ、BNT、moderna等各家疫苗都是在完成三期期中試驗結果後,確認試驗結果符合特定標準後,才獲得主要國家緊急授權(EUA)。
王婉諭統整,AZ、BNT、moderna等3種疫苗,皆是在去年底發布超過上萬人的三期試驗期中數據報告,獲得美國或英國主管機關通過的緊急使用授權;因此,王婉諭表示,海外合格的主要疫苗,沒有只做二期試驗就得到EUA。
對於指揮中心說國產二期就有可能拿到EUA,以及可能的問題?王婉諭表示,三期疫苗試驗非常昂貴,除了美、英之外,沒有其他國家有在這麼短時間製造疫苗,且在有效疫苗問世後,新的疫苗也不適合在臨床實驗給受試者打鹽水做對照,會有倫理問題,因此透過已獲認證的疫苗作標準,尚未進入三期臨床的疫苗,根據中和抗體比較,只要能產生足夠的抗體即可證實他的保護力。
王婉諭解釋,這就是WHO 近期開始討論的「免疫橋接實驗」,包含 WHO 和歐盟,正制定一個「抗體保護力(COP)」標準,讓中和抗體評估可以成為一種認證標準。
然而,王婉諭表示,國產疫苗連二期試驗都還沒解盲,而WHO也還沒提出「抗體保護力(COP)」標準,而且過去發生初期人體試驗有效,大規模臨床試驗無效的情形發生許多,衛福部長陳時中也曾提過,「國產疫苗目前是打算要用中和抗體的比較去確認有效性,確實比較不完整」、「國產的安全性、有效性仍需要專家和科學的驗證。」
最後,王婉諭強調,國產疫苗具有高度戰略價值,因為病毒未來很可能持續變異,每年都要需打新的一劑,甚至研發新的技術,而台灣的國際處境,也需要擁有自給自足的技術,而國內研發廠商高端與聯亞都有對外透露將進行三期臨床試驗,因此樂見國產疫苗在三期臨床試驗並取得相關研究結果。
但是,王婉諭提醒,執政黨不應該在國產疫苗還沒完成二期解盲的情況下,就納入台灣8月會取得的1000萬劑疫苗當中,「仿佛像一個連期中考都還沒完成的學生,卻事先拿到成績一樣」,也讓國人陷入健康風險,也有可能未來施打後無法在國境間移動,更不應該將民眾的健康視若罔顧,為此仍應透過公私協力,儘速取得獲國際認證疫苗。
相關新聞請見︰
「武漢肺炎專區」請點此,更多相關訊息,帶您第一手掌握。













