藍委狂打高端流感疫苗 食藥署:審查標準都一樣!

食藥署副署長陳惠芳強調,目前已核准的六項四價流感疫苗,皆依相同標準進行審查。(記者邱芷柔攝)
〔記者邱芷柔/台北報導〕國民黨籍立委王鴻薇大動作召開記者會,質疑高端公司的四價流感疫苗,在台灣沒有進行完整的三期臨床試驗,且實驗對象和目前接種人群不符,恐有安全疑慮,並指衛福部不公開相關審查資料,把「商業機密」看得比人民健康還重要。對此衛福部食藥署今(18日)在例行記者會上說明四價流感疫苗查驗登記流程,並強調,目前已核准的六項四價流感疫苗,皆依相同標準進行審查。
針對王鴻薇指高端疫苗在台灣三期臨床只有做20至50歲族群,收案不夠完整等質疑,食藥署副署長陳惠芳說明,只要有亞洲族群的試驗,就不會要求必須在台灣做臨床試驗,且該疫苗在韓國核准6個月以上就可使用,台灣更嚴格,只核給3歲以上和成人使用。
陳惠芳進一步說明,高端臨床試驗資料檢附了在韓國執行的第一、二期及第三期臨床試驗,受試者年齡為3至18歲、19歲以上及65歲以上,並於國內執行第三期臨床試驗,受試者年齡為20歲至50歲,綜合韓國及台灣臨床試驗結果,可支持其療效及安全性。
陳惠芳說,臨床試驗並未限定執行地點,是看廠商提供的整體臨床試驗數據結果進行審查療效及安全性,並依ICH E5所訂的銜接性試驗基準審視該藥品是否具有族群差異,若經評估「無族群差異」,就可以引用國外臨床試驗數據資料,不會要求要在台灣執行臨床試驗或執行全年齡層的臨床試驗,以減少重複進行臨床試驗。
陳惠芳強調,其他已核准的流感疫苗,也因評估無族群差異,同樣都沒有在台灣執行臨床試驗或全年齡層臨床試驗。
對於高端申請審查時提供的資料未公開,陳惠芳也說,依據「藥事法」第40條之1及營業秘密法第2條規定,藥品查驗登記時所檢附原始數據屬「營業秘密」資料,食藥署應保密,不能對外公開。
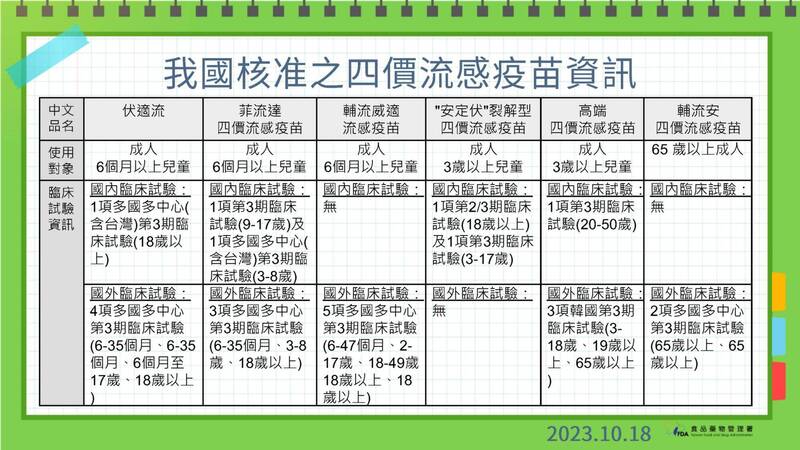
食藥署公開目前已核准的六項四價流感疫苗資訊,強調皆依相同標準進行審查。(記者邱芷柔翻攝)











