美FDA完全核准輝瑞疫苗
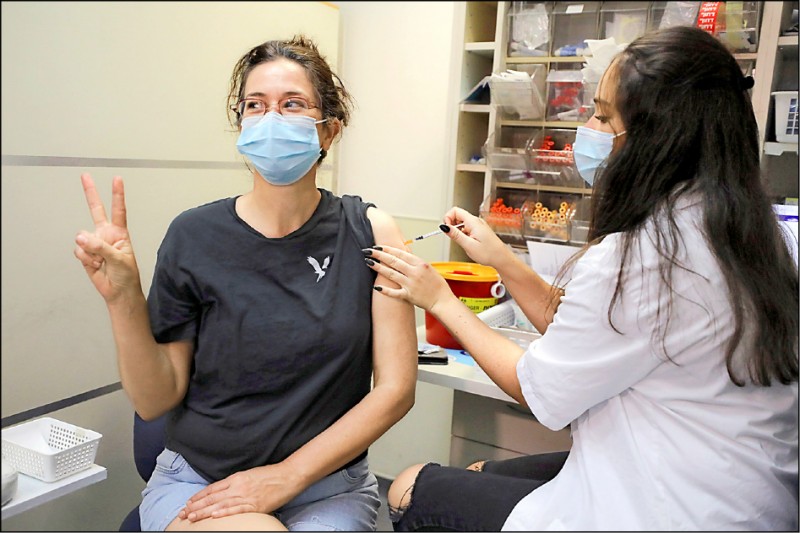
以色列十九日開放四十歲以上成年人接種第三劑疫苗,圖為一名婦女二十日在耶路撒冷接種第三劑疫苗。(路透)
16歲以上適用 12至15歲緊急授權
〔編譯黃靖媗/綜合報導〕美國食品暨藥物管理局(FDA)廿三日正式完全核准輝瑞/BNT疫苗,適用於十六歲以上人口接種,成為美國首支獲得完全授權的武漢肺炎疫苗,可望提高民眾對疫苗施打的信心;而在十二至十五歲兒童方面,輝瑞/BNT疫苗仍只有緊急授權。
以色列︰長者打3劑 重症保護力增
FDA科學家檢視數十萬頁的疫苗數據,FDA代理局長伍考克(Janet Woodcock)表示,輝瑞/BNT疫苗符合FDA要求的安全、有效性,與製造品質的高標準。輝瑞藥廠表示,向FDA呈交在美國、歐洲、土耳其與南非等地共四.四萬名臨床試驗受試者的數據,顯示輝瑞/BNT疫苗在預防感染上有九十一%的效力,略低於FDA去年十二月批准緊急使用授權時的九十五%。
此外,FDA也已緊急授權為免疫系統脆弱族群注射第三劑輝瑞或莫德納疫苗。
以色列方面,以國衛生部廿二日發表的報告也指出,施打第三劑輝瑞/BNT疫苗,可顯著提升已施打兩劑的六十歲以上長者對感染武漢肺炎及惡化為重症的保護力,但研究的完整細節尚未公開。衛生官員分析來自以色列格特納研究所(Gertner Institute)與KI研究所(KI Institute)的統計數據後,發現六十歲以上長者在接種第三劑疫苗的十天後,對抗感染的保護力提升至只接種兩劑者的四倍,對重症與住院的保護力也提升至只接種兩劑者的五至六倍。
以國政府指出,接種第二劑疫苗至少五個月後,才能接種第三劑疫苗。衛生部的數據顯示,已有逾一百四十萬名以國民眾接種第三劑疫苗。以色列已於七月三十日起,為六十歲以上長者接種第三劑疫苗,十九日開放四十歲以上成年人、孕婦、教師與醫護人員接種追加劑。















