政府預購500萬劑聯亞 三期若過仍算數
〔記者林惠琴、邱芷柔、蘇金鳳、陳永吉/綜合報導〕國產聯亞疫苗的緊急使用授權(EUA)未通過,但中央流行疫情指揮中心表示,政府預採購的五百萬劑疫苗未必不算數;若聯亞經第三期臨床試驗證明具有保護力,仍可望適用。至於已生產的兩百多萬劑,效期長達兩年,屆期前若可驗證效力,返台申請藥證通過,未必全數作廢。
聯亞:三期是否執行待評估
不過,聯亞新冠疫苗二期試驗計畫主持人、中國醫藥大學附設醫院副院長黃高彬表示,衛福部雖已同意直接做第三期,第三期若通過就直接核准,他原本也是規劃希望第三期的臨床試驗在台灣及印度一起做。但由於第三期所需費用相當高,廠商需要進一步討論思考再決定。
聯亞生技子公司聯亞藥昨日代母公司聯亞生技在公開資訊觀測站公告表示,聯亞生技將重新執行第三期臨床試驗之效益評估。
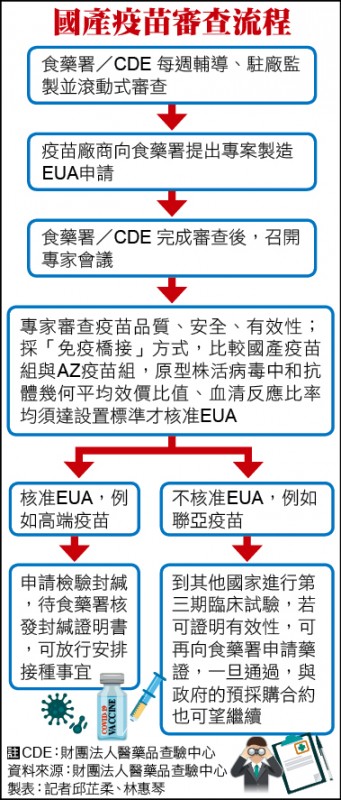
醫藥品查驗中心醫師詹明曉說明,目前國產疫苗療效評估方法與取得EUA的標準,經專家會議決定以「免疫橋接」方式,比較國產疫苗組與AZ疫苗組六十五歲以下成年受試者於第二劑施打後二十八天的血清中和抗體值,必須達到兩項條件,其一是原型株活病毒中和抗體幾何平均效價比值的九十五%信賴區間下限須大於○.六七,若AZ組為一,國產疫苗組就要達到○.六七倍,也就是不低於AZ組三分之二算過關。
其二是血清反應比率九十五%信賴區間下限須大於五十%。簡單地說,考量疫苗至少要有六成保護力,因此將AZ組每人出現的血清反應濃度由高往低排,以一百名為例,取第四十名為基準,等於贏過六十人,國產疫苗至少要有五十%達到這個濃度數值才算通過。
對於聯亞相關數據,指揮中心指揮官陳時中指出,沒通過原則上不公布,尊重廠商的決定。
聯亞:T細胞反應也很重要
黃高彬則認為,疫苗不是只有中和抗體,還有T細胞反應的問題,食藥署訂出來的標準只討論中和抗體,而聯亞的T細胞反應是很好的。聯亞生技也強調,聯亞疫苗可有效誘導T細胞毒殺病毒免疫力與B細胞對病毒產生中和性抗體,中和性抗體效價持久,且可中和大多數變異株。
聯亞藥股價10多分鐘跌4成
聯亞藥股價昨日暴跌,十餘分鐘內從二○三元一路跌至最低一○○元,終場收在一一七.五元,跌幅逾四成。
聯亞藥的大股東之一台塑生醫,上週五及昨日也處分聯亞藥持股二七九一張,從聯亞藥掛牌以來,賣股超過一萬張,持股比重從十五%降至不到五%,獲利相當可觀。