適20歲以上成人施打 高端疫苗 獲准生產
〔記者邱芷柔/台北報導〕衛福部食藥署昨宣布,高端疫苗研發的MVC-COV1901武漢肺炎疫苗,中和抗體與血清反應率均達到審查標準,且安全無虞,因此核准通過緊急使用授權(EUA),高端疫苗將可專案生產,適用於二十歲以上成人接種兩劑,預計八月就可開始少量供應;這不僅宣告國產COVID-19疫苗將正式問世,也是我國第一個「專案製造」的疫苗。
八月開始 少量供應
我國此次以「免疫橋接」方式進行審查,食藥署招募兩百名部立桃醫醫護人員接種兩劑AZ疫苗,並抽取血清分析作比較,要求國產疫苗的抗體效價不能比AZ差。
高端疫苗六月十日公布二期臨床試驗解盲數據,並申請EUA審查;食藥署前天邀集藥學、毒理學、臨床醫學、公衛、法律等領域專家開會審查,正式通過高端疫苗EUA申請。
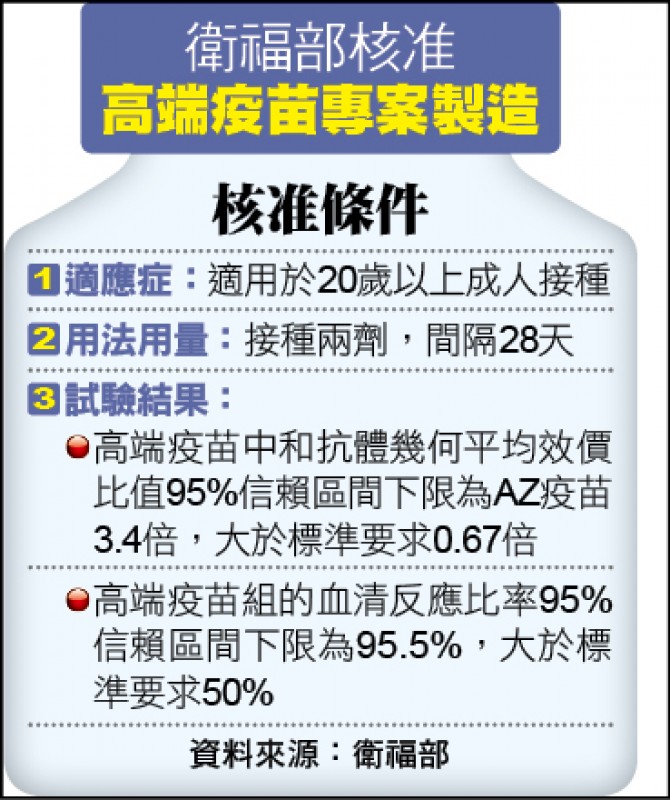
食藥署長吳秀梅指出,通過EUA主要依據有兩項,實驗數據顯示,高端疫苗的原型株活病毒中和抗體效價比值(GMTR),為AZ疫苗的三.四倍,遠大於審查標準要求的○.六七倍;此外,以AZ疫苗施打者前四十%在疫苗施打後血清反應率為基準,高端疫苗的血清反應比率九十五.五%、亦即逾九十五%施打者都可達到,也大於審查標準要求的五十%。
接種兩劑 間隔28天
此次與會專家共二十一人,主席不參與投票,有十八人同意、一人希望補件再議,僅一人不同意;食藥署最後依藥事法規定,核准高端疫苗專案製造,適用二十歲以上成人接種兩劑,間隔二十八天。
此外,專家會議也建議,高端疫苗於專案核准製造期間,藥商須每月提供安全性監測報告,並於核准後一年內檢送國內外執行疫苗保護效益報告,以保障國人用藥安全。
政府對兩家國產疫苗分別預採購五百萬劑,取得EUA才能合約生效。中央疫情指揮官陳時中昨也表示,後續還需經ACIP(傳染病防治諮詢會預防接種組)審議通過,高端才能納入公費疫苗施打計畫。