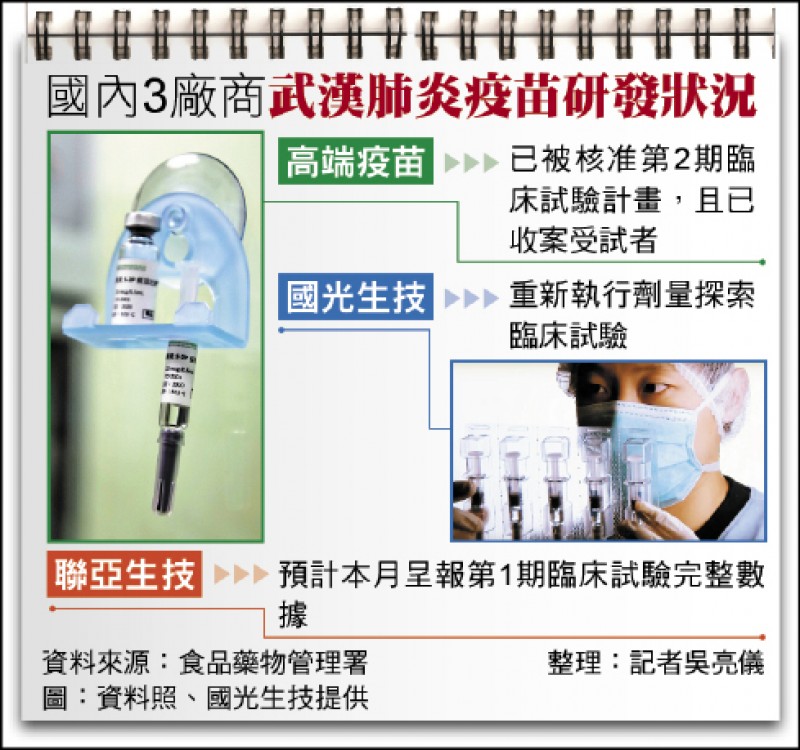
國衛院︰國產武肺疫苗 年中有望緊急授權
2021/01/16 05:30
高端啟動二期試驗 找3千名受試者
〔記者吳亮儀/台北報導〕國內目前有國光、高端和聯亞三家生技廠商正加緊研發武漢肺炎(新型冠狀病毒病,COVID-19)疫苗,去年底,食藥署宣布核准高端公司的疫苗展開第二期臨床試驗;國家衛生研究院預估,今年中有望申請緊急使用授權。
我國積極爭取向國際生技大廠購買武漢肺炎疫苗,盼能在今年第一季開始施打,也輔導國內廠商積極研發,目前高端公司的疫苗已可啟動第二期臨床試驗計畫。
國衛院副院長司徒惠康昨出席國衛院與多家藥廠簽署「精準醫療合作聯盟協議書」儀式,會後受訪表示,疫苗二期臨床試驗開始執行後,今年中應該就可申請緊急使用授權。
他指出,正常來講,第二期臨床試驗僅需幾百名受試者,但台灣走的是「加強版」二期試驗,找三千名受試者接受試驗,且要在P3等級實驗室確認受試者體內可有足夠的中和抗體。
目前國內三家生技廠商中,僅一家可進展到第二期臨床試驗,司徒惠康指出,疫苗施打有兩大重要原則,第一是安全性,另一個是保護效果。台灣沒有那麼多病例,因此第一期到第二期臨床試驗的過程要求更是嚴謹。
他表示,我食藥署、醫藥品查驗中心(CDE)等單位都密切管控,在所有條件都符合的情況下,才能往下一階段,相信另兩間廠商也有機會很快進展到第二期臨床試驗計畫。
疫苗效力規定逾5成 目標是越高越好
至於疫苗的防護效力,目前根據各國公布的相關資訊,五十%至九十%都有,國產疫苗的標準要達到幾%才算合格?國衛院院長梁賡義表示:「目前的規定是至少要五十%,對民眾而言,當然是越高越好。」
食藥署長吳秀梅指出,高端公司在去年底就已收案第一名受試者,現也陸續收案中,食藥署積極輔導各家生技廠商做人體試驗的行政流程,一有行政問題,會馬上派員協助。